
Leitfaden zur Messung des pH-Werts von Lebensmitteln

Chemischer Sauerstoffbedarf CSB – photometrisch bestimmt

Die CAL Check- Funktion für Photometer richtig nutzen

Die Gro Line-Serie

Honigsorten anhand ihrer Leitfähigkeit unterscheiden
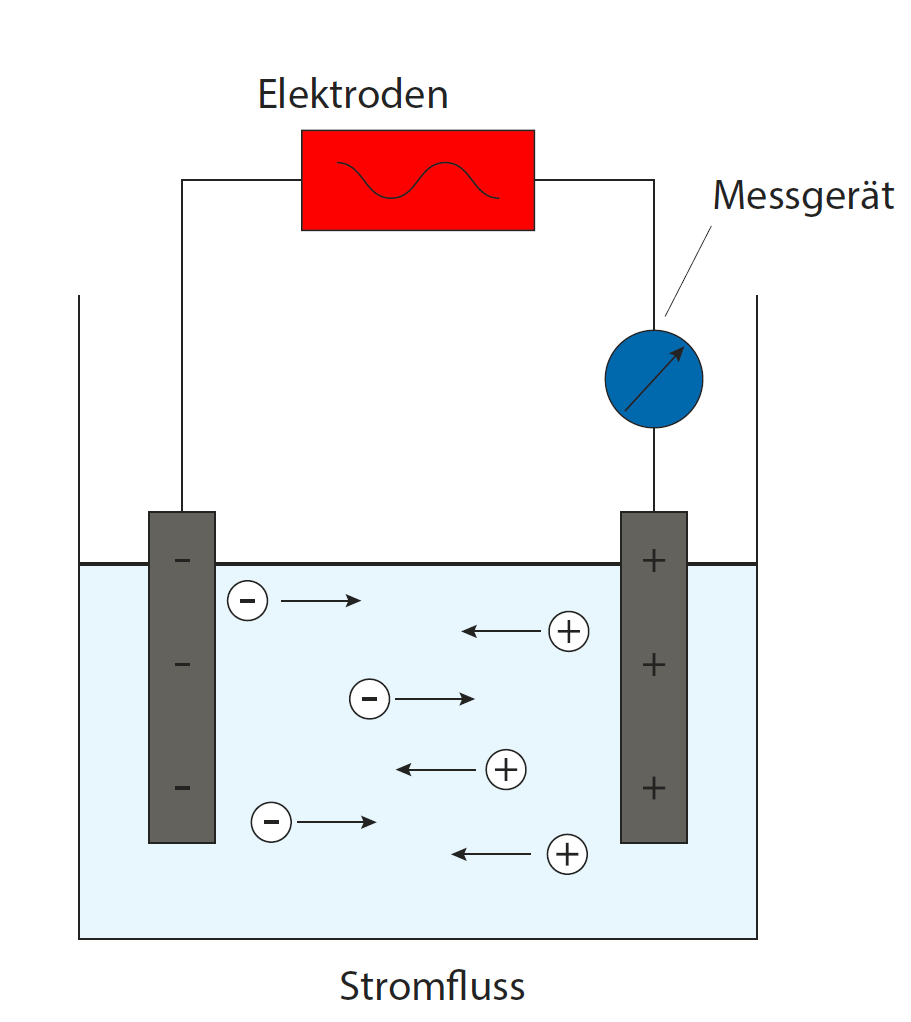
Leitfähigkeit erklärt

Leitfähigkeitsmessung, -kalibrierung und Elektrodenpflege

pH in Fleisch sicher und professionell messen

Warum sind die vielen Lösungen bei der pH-Messung wichtig?

Bedarfsgerechte Umweltanalytik dank moderner Photometer

Das erste Spektralphotometer von Hanna Instruments

Den pH-Wert in Wein und Maische messen

Den pH-Wert von Lebensmitteln messen

Den Säuregehalt in Fruchtsaft bestimmen

Der GroLine®-Monitor für pH und Leitfähigkeit

Der pH-Wert von Mascara

Die Bedeutung des pH-Werts bei der Käseproduktion
Die neuen Foodcare Thermometer von Hanna Instruments

Die richtige Wassertemperatur zum Kaffee brühen

HI833xx Multiparameter-Photometer mit pH-Meter

Interessantes rund um die Zuckergehaltmessung in Traubenmost

Neue HALO®-pH-Elektroden in Hannas Sortiment

Professionelle Messtechnik in den Einsatzfeldern Trinkwasser, Hydrogeologie und Limnologie

Redoxpotential messen

Refraktometrie

Temperaturmessung und Thermometer
Titrimetrische Calcium-Bestimmung mit der ionenselektiven Elektrode

Was hat die Hygiene in Schwimmbädern mit dem Redoxpotential gemein?

Alkalinität im Meerwasseraquarium / Riffaquarium messen

Calcium – ein wichtiges Element im Riffaquarium

Die Wassertemperatur im Aquarium

Fehler bei der Leitfähigkeitsmessung

Hanna Combo
Hannas Foodcare pH-Meter

pH-Messung in nichtwässrigen oder teilwässrigen Medien

Photometrische Messungen für Meerwasseraquaristik

Praktische Redoxpotentialmessung - Teil 1, chemische Vorbehandlung

Praktische Redoxpotentialmessung - Teil 2, Umgang mit der Elektrode

Warum ist es wichtig, den pH-Wert in Aquarienwasser zu messen?

Wussten Sie, dass der pH-Wert auch beim Backen von Keksen wichtig ist?

Acht Hinweise, um das Beste aus Ihrem Checker® HC herauszuholen

Die CAL Check-Funktion
Die Messung der Gesamthärte

Die richtige pH-Kalibrierlösung finden

Ein Hydroponik-Monitor auf Abwegen

Gesamtammonium im Aquarium
Grundlagen der Spektralphotometrie

Nitrit im Salzwasseraquarium bestimmen

Phosphor im Riffaquarium messen

Unsere Pool Line - eine kleine Kaufberatung
pH-Wert und pH-Elektrode – etwas Theorie

Abgeleitete Parameter der Leitfähigkeit

Aufschlämmung für die pH/Leitfähigkeitsmessung von Boden herstellen

Messgeräte ohne pH-Elektroden verfügbar

Wasserwerte in Heizungswasser bestimmen

Analytik ist nicht Ihr Bier?

Das Messen des Säuregehalts in natürlichen Gewässern

Den Gehalt an Nitrationen mit der ISE messen

Den Reifegrad von Tomaten bestimmen
Den Wassergehalt von Biodiesel bestimmen

Der neue HI98319 Salinitätstester von Hanna Instruments

Die Analyse von Met

Die Leitfähigkeit von Boden bestimmen

Die neue HI97xxx-Serie

Gelöster Sauerstoff – Anwendungen und Messmöglichkeiten

HI935012 – Ein Thermistor-Thermometer für Brauprozesse

HI98198 opdo - Unsere Messgeräte-Serie bekommt Zuwachs

HI99xxxx-Serie in neuem Design
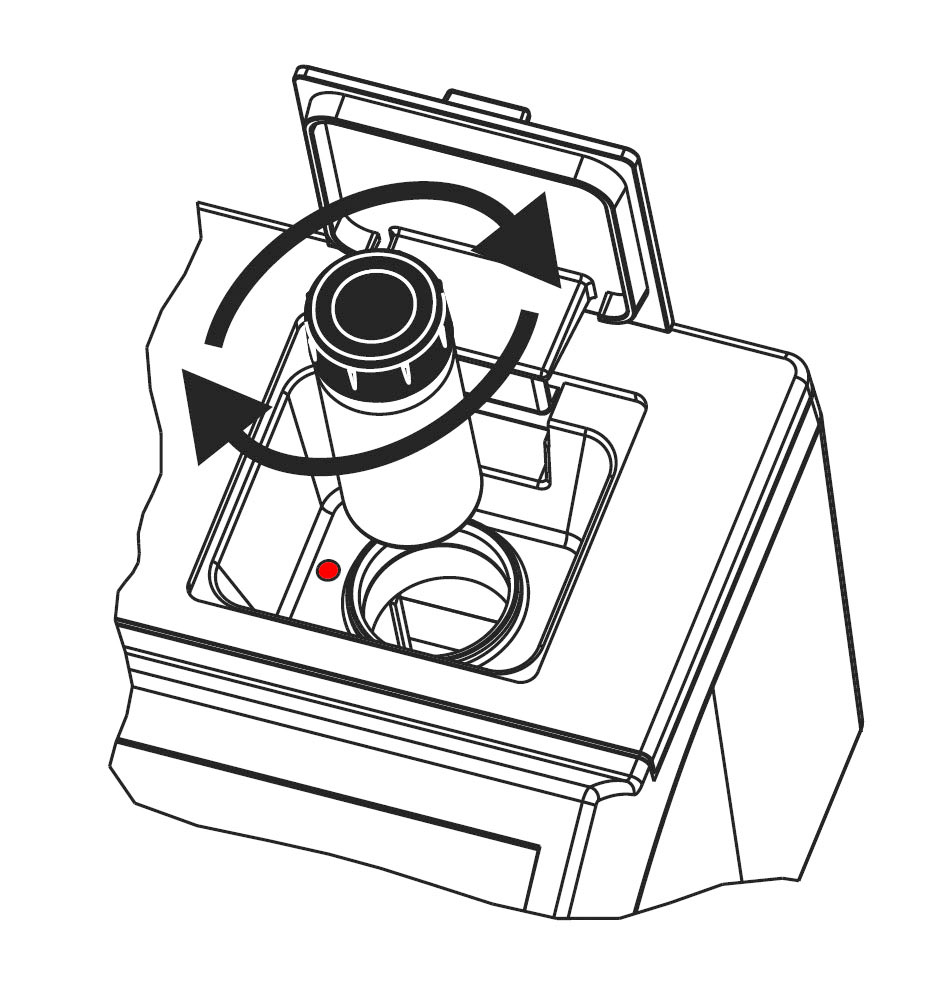
Küvetten richtig für die Trübungsmessung vorbereiten

Neue Messgeräte in der HI9816x-Serie
Neue Tester von Hanna Instruments
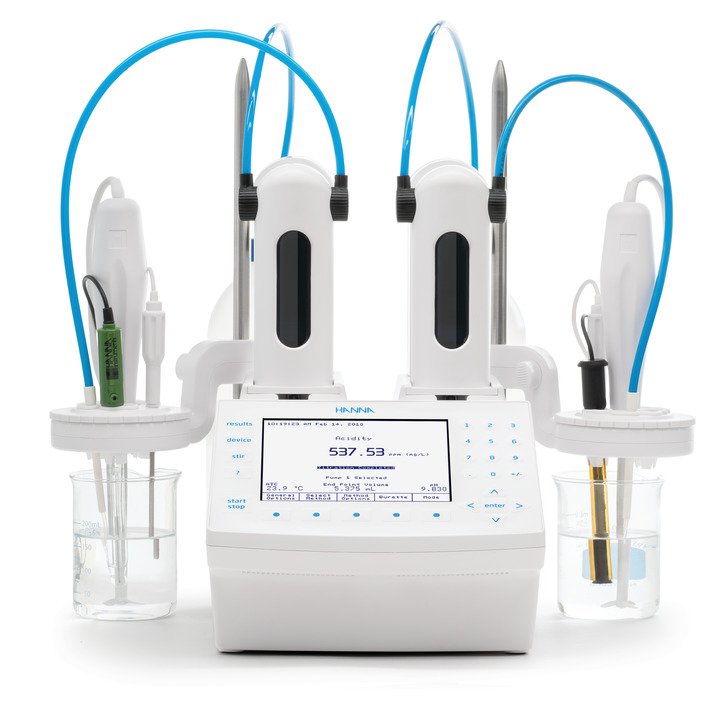
Neue Titrationssysteme HI931 - HI932C1 – HI932C2

Salinität in Meerwasseraquarien messen

Tipps & Tricks zu photometrischen Messungen

Trübungsmessung bei der Zuckerherstellung

Warum es wichtig ist, den Gesamtgehalt gelöster Feststoffe in Kaffee zu bestimmen

Was ist eigentlich gelöster Sauerstoff?

Bestimmung von pH-Wert und titrierbarer Säure in Sauerteig

Das HI98199 ergänzt die Serie an Outdoor-Messtechnik perfekt

Den Brechungsindex von Marmelade, Konfitüre und Co. messen

Den pH-Wert des Bodens bestimmen
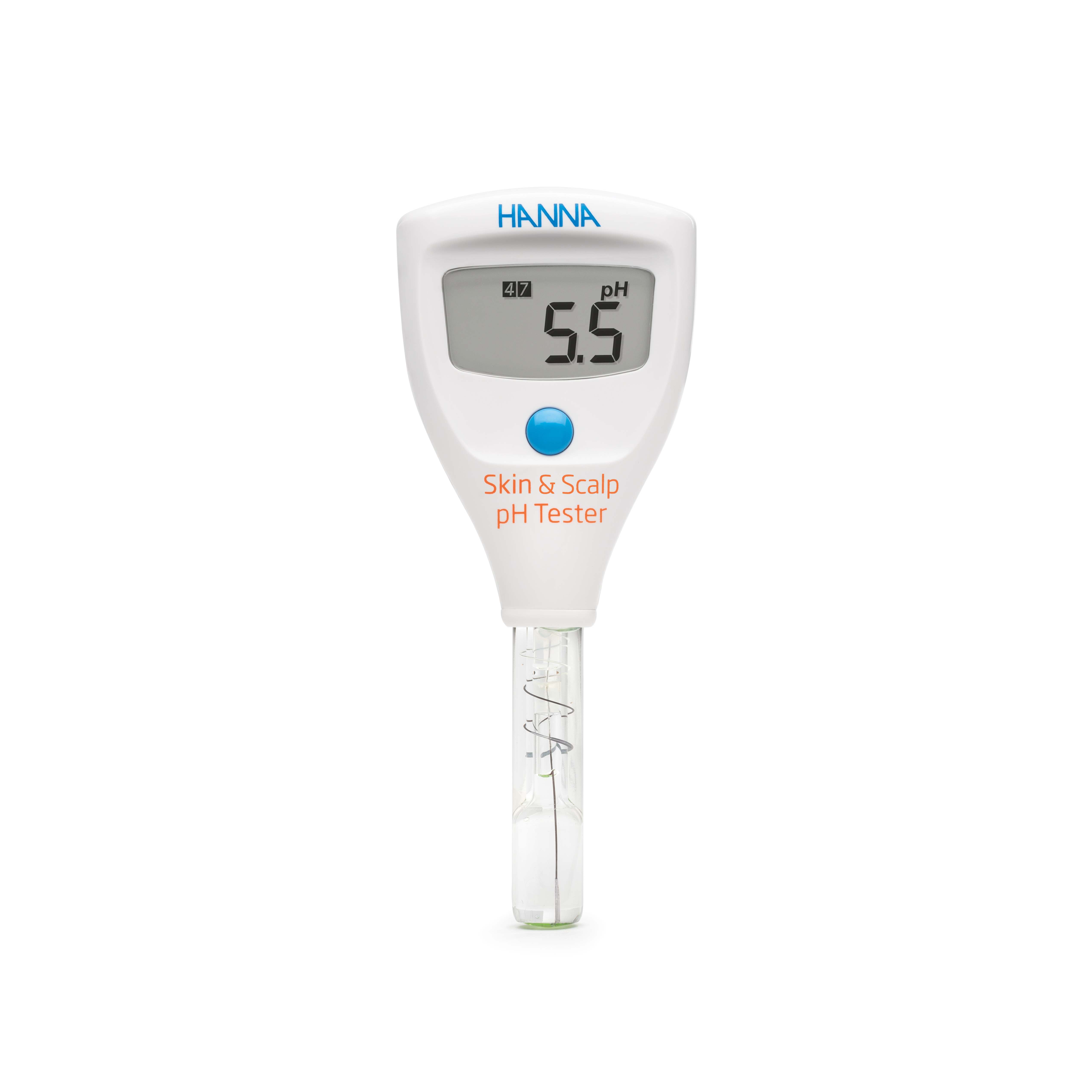
Der HI981037 pH-Tester für Messung direkt auf Haut

Der pH-Wert in Joghurt

Der pH-Wert in Milch

Der pH-Wert von Käse

Die Luftfeuchtigkeit - ein wichtiger Faktor für unser Wohlbefinden

Gelöste Sauerstoffmessung – Worin liegen die Vorteile eines optischen Systems gegenüber einem galvanischen System?

HI10532 HALO® Bluetooth-pH-Elektrode für Lebensmittel

HI144 / HI144-10 Temperatur-Logger
![HI151-x[xx] Pocket Thermometer Checktemp® 4](https://hannainst.de/media/a4/2a/48/1681390725/HI151_Gruppenbild.jpg?ts=1681390725)
HI151-x[xx] Pocket Thermometer Checktemp® 4

HI713 oder HI736 Phosphor, Phosphat – ja was denn nun? Hier erklären wir Ihnen, wann Sie was in Ihrem Riffaquarium messen sollten

HI774 Checker® HC für Phosphat (ultra niedriger Bereich), speziell für Meerwasser

Inhaltsstoffe in Trinkwasser – Calcium- und Magnesiumkarbonat

Kennen Sie eigentlich schon unsere Schutzhüllen für Ihre Messgeräte?

Kolostrumqualität bei Mutterkühen überprüfen

Ostafrika-Buntbarsche – die Spezialisten unter den Aquarienfischen

Temperaturmessung bei der Lebensmittel- und Getränkeherstellung

Tipps & Tricks zu Messungen mit Ihrem Salinitätstester HI98319
Warum kann es sinnvoll sein eine Wasserprobe in der Photometrie vor der Messung zu filtrieren?

Das Textil-Diaphragma bei pH-Elektroden

Der HI981421 GroLine® -Monitor für die Hydroponik mit Inline-Sonde
Drahtlos messen mit der Hanna Lab App

HI148-x Thermologger

Salz- und Säureanalysen in Lebensmitteln
Tipps zur Verwendung von Mini-Hubkolbenpipetten (Analysenpipetten)

Wichtige Wasserwerte für Aquarien und womit Sie sie messen können

Chemische Parameter von Fischgewässern

Der pH-Wert bei der Reinigung von Wolle und anderen tierischen Fasern

Die Alkalinität - ein wichtiger Wasserparameter

Die Bedeutung von pH-Wert und Leitfähigkeit bei der Pflanzenbewässerung und Fertigation

Die Bestimmung des pH-Wertes in Wein

Die pH-Wert-Messung in Sushi-Reis

HI90060X-Serie Photometrische Elektroden
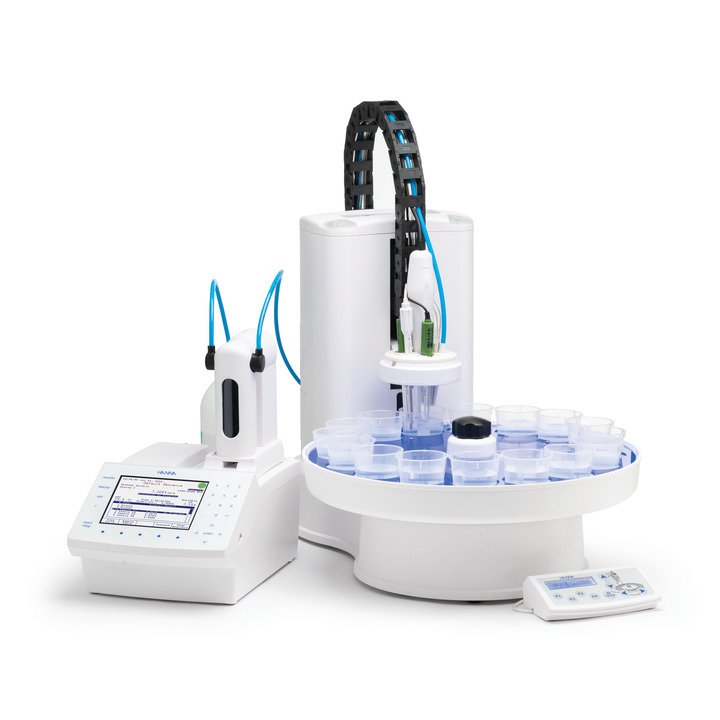
HI922 - Hannas automatischer Titrationsprobenwechsler
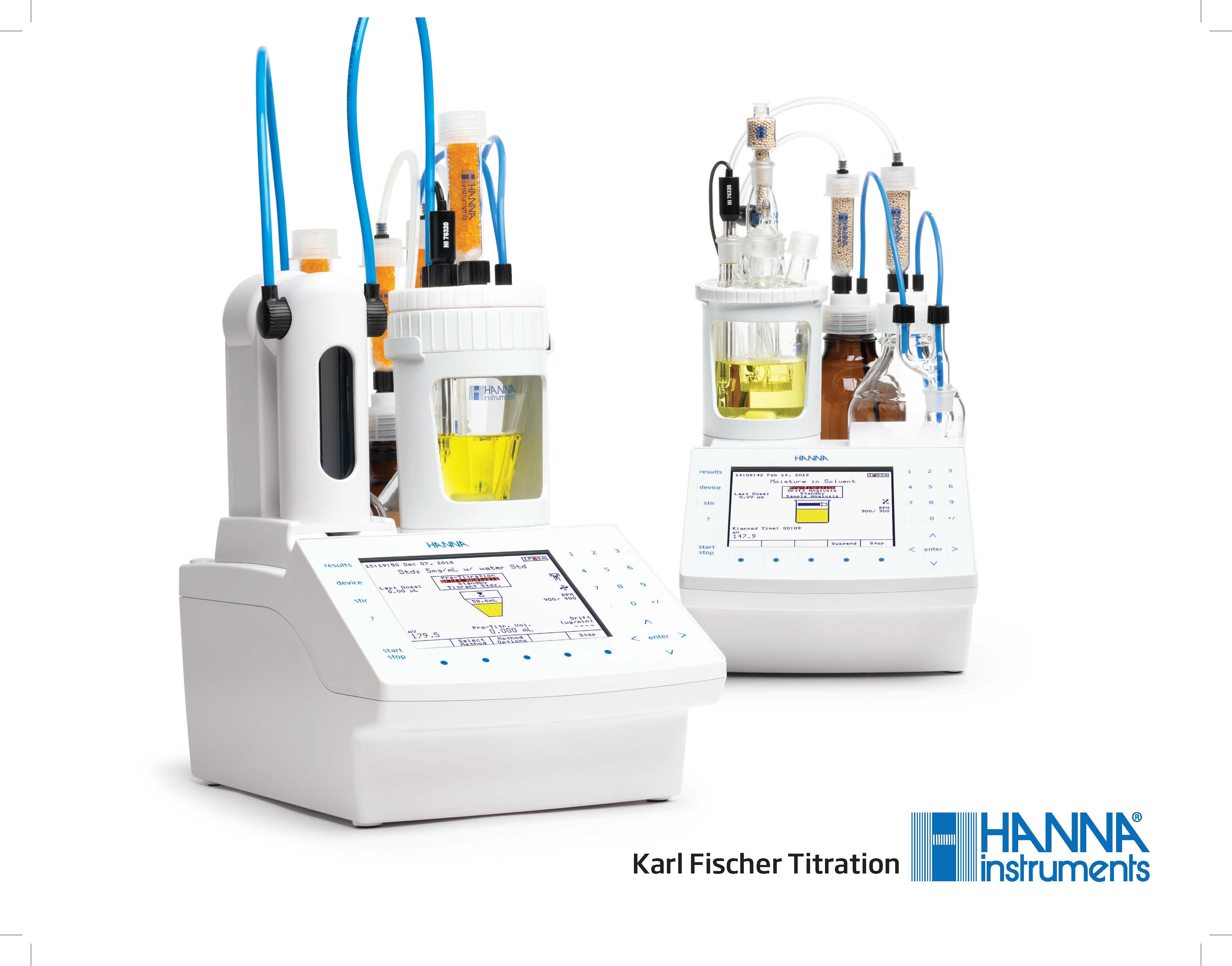
HI93x – Hanna Instruments Karl Fischer Titratoren
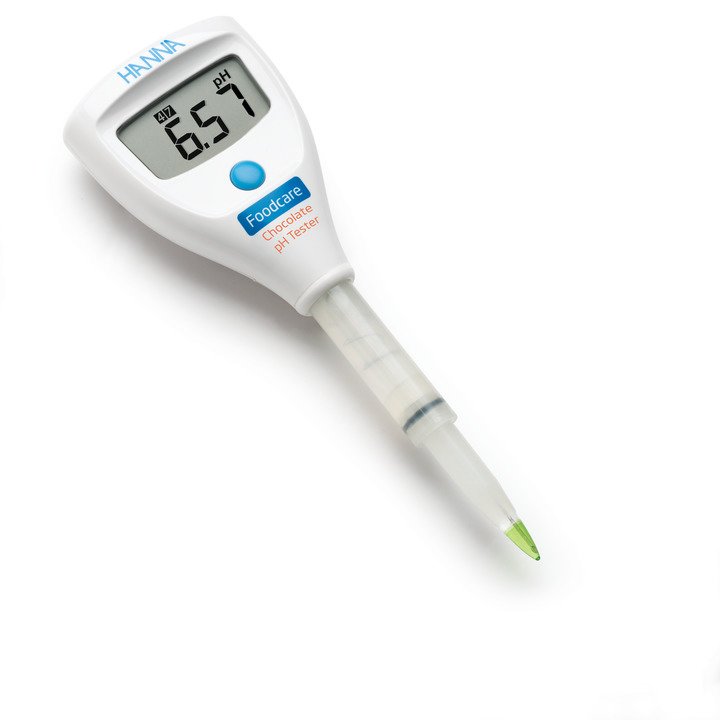
HI98103x-Serie um zwei Tester erweitert
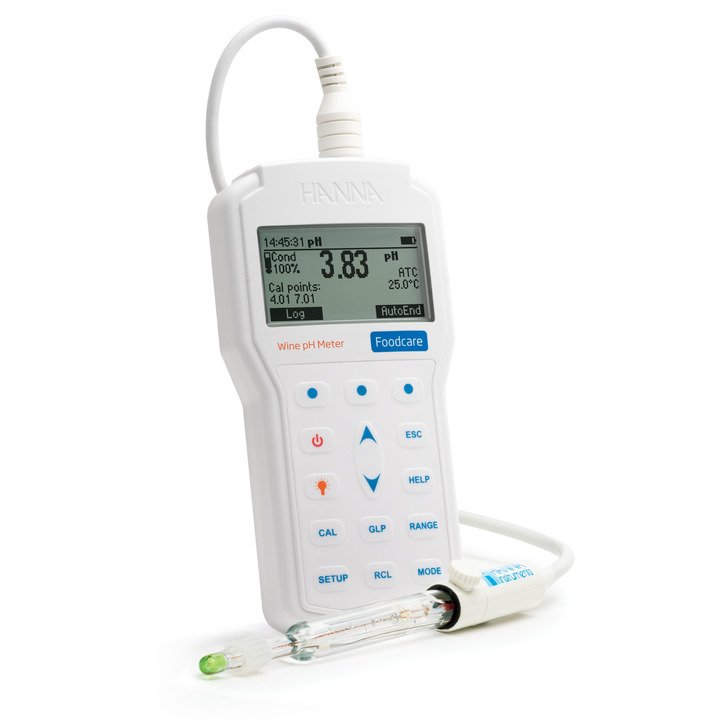
HI98169 Foodcare-pH-Meter für die Weinanalyse

Kontrolle wichtiger Wasserparameter in geschlossenen und offenen Kühlkreisläufen

Moderne Messtechnik für die Lebensmittelsicherheit

Neues für die Pool-Branche

Photometer-Serie HI97xxx erweitert

Refraktometrische Wassergehaltsbestimmung in Honig

Relevante Parameter im Abwasser bestimmen

Abwassereinigung und Messung wichtiger chemischer Parameter im Klärwerk

Bestimmung der Alkalinität in Wasser durch Titration

Chemischer Sauerstoffbedarf in Abwässern mit hoher Trübung

Das HI98494 Portables Multiparameter- pH/EC/OPDO®-Messgerät mit Bluetooth®-Technologie

Den Säuregehalt mit HI931 in Fruchtsaft bestimmen

Der Biochemische Sauerstoffbedarf (BSB) – ein Wert zur Beurteilung der Effizienz der Abwasserbehandlung

Die Bedeutung der Wasserqualität bei der Haltung von Zebrabärblingen für die Forschung

Die Bestimmung von CSB in Abwasser

Genaue Leitfähigkeits-Bodenuntersuchungen leicht gemacht

Hefe-assimilierbarer Stickstoff (YAN) – essenzieller Hefenährstoff für gesunde Weingärungen

HI780 Checker® HC pH in Meerwasser
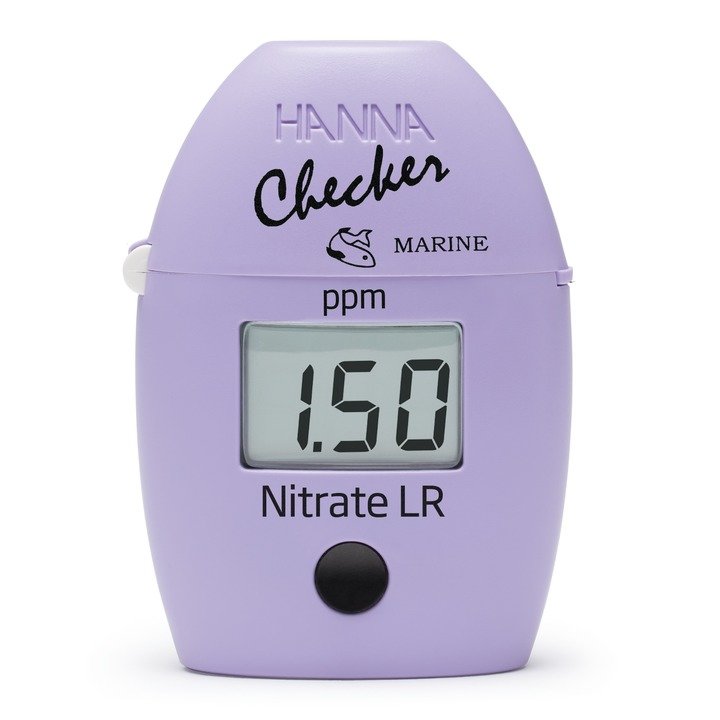
HI781 Checker® HC Nitrat in Meerwasser

Nitrat in Meerwasser mit dem HI781 richtig bestimmen

pH-Wert und gelöster Sauerstoff im Abwasser-Belebungsbecken

Überwachung der Nitratauswaschung aus gedüngten Böden

Überwachung und Steuerung des pH-Wertes von Industrieabwasser

Wenn es blitzsauber sein muss - Wirkung und Bestimmung von Desinfektionsmitteln

Zuckergehalt von Fruchtsäften refraktometrisch bestimmen

„Nitritpeak“ in Aquarien erkennen und Schäden vorbeugen

Cyanursäure in Schwimmbadwasser messen

Konzentration ist alles - die Wirksamkeit von Natriumhypchloritlösungen refraktometrisch bestimmen

Phosphorwerte im Riffaquarium ermitteln

Warum Alkalinität und Calcium in Riffaquarien besonders wichtig sind

Das Redoxpotential - ein wichtiger Parameter bei der Pooldesinfektion

Der pH-Wert im Pool - das A und O für die Wasserqualität

Haut-pH-Wert messen leicht gemacht

HI782 Checker® HC Nitrat im Meerwasser, hoher Messbereich

HIREEF-2 | Das Rundum-Sorglos-Paket für Ihr Riffaquarium

Individuelle Kosmetik: Der pH-Wert macht's

Ionenkonzentration und Photometrie zur Wasserhärtebestimmung

pH-Wert-Messung von Hautpflegeprodukten leicht gemacht

Ascorbinsäure (Vitamin C) und photometrische Titration

Das HI97105 Photometer für Meerwasser-Aquaristik

Die Alkalinität bei der Wasseraufbereitung

Die Bedeutung des pH-Werts beim Bierbrauen

Die Leitfähigkeit von Joghurt

Die Leitfähigkeit von Umkehrosmosewasser

Die verschiedenen Arten von Phosphor und womit Sie sie messen können

FAQ - Die 8 häufigsten Fragen zu Ihrem Multiparameter-Messgerät
Gesamtchlor und Freies Chlor – was ist eigentlich der Unterschied?

HALO2 mit Bluetooth® Smart-Technologie

Manuelle oder automatische Titration? Ein ehrlicher Vergleich

Mehr als nur Testkits - pH-Wert & Desinfektion in Pools bestimmen & regeln

Monitor für Meerwasseraquarien
Standardisierung von Titranten für die genaue Karl-Fischer-Titration

Tipps zur pH-Wert-Messung, -Kalibrierung und Elektrodenpflege

Titrierbare Gesamtsäure in Wein messen

Temperaturüberwachung bei Lagerung und Transport von Fleisch

Wasserqualität von Fischgewässern - Teil 2: Sauerstoff

Wasserqualität von Fischgewässern - Teil 3: Elektrische Leitfähigkeit

Wasserqualität von Fischgewässern - Teil 1: pH-Wert

10 Best Practices für Ihre volumetrische Karl-Fischer-Titration

Titrimetrische Calcium-Bestimmung mit der ionenselektiven Elektrode
Verwendung einer ioneselektiven Elektrode ISE zur Bestimmung des Calciumgehalts. Hier aufgezeigt am Beispiel Nahrungsergänzungsmittel.
 In diesem Artikel diskutieren wir den Einsatz einer ionenselektiven Elektrode (ISE) für Calcium zur Konzentrationsbestimmung dieses Elements. Zur besseren Illustration verwenden wir die Untersuchung von Nahrungsergänzungsmitteln.
In diesem Artikel diskutieren wir den Einsatz einer ionenselektiven Elektrode (ISE) für Calcium zur Konzentrationsbestimmung dieses Elements. Zur besseren Illustration verwenden wir die Untersuchung von Nahrungsergänzungsmitteln.
Calcium – eines der wichtigsten Minerale für die Gesundheit
Calcium spielt eine wesentliche Rolle in unserer Gesundheit und ist das am häufigsten vorkommende Mineral in unserem Körper. Es hilft uns Zähne und Knochen gesund zu erhalten, reguliert die Muskelkontraktion und unterstützt die Freisetzung von Hormonen und Enzymen. Somit führt eine Unterversorgung mit Calcium z.B. zu Muskelverkrampfung, Verwirrung und niedriger Knochendichte. Eine Überversorgung hingegen kann zu Nierensteinen und Ablagerungen in Blutgefäßen führen. Verschiedene Gesundheitsorganisationen empfehlen eine Aufnahme vom 1000 mg Calcium täglich für Erwachsene.
Die wichtigste natürliche Quelle für Calcium sind Milch und Molkereiprodukte. Dies bringt ein Problem für Menschen, die auf Milchprodukte verzichten, mit sich. Zwar gibt es Gemüse mit vergleichsweise hohem Calciumgehalt, wie Blattkohl, Wildbrokkoli und Grünkohl, der Verzehr von diesen alleine reicht aber in der Regel nicht für eine ausreichende Versorgung. Um gesund zu bleiben nehmen daher viele Veganer calciumhaltige Nahrungsergänzungsmittel zu sich.
Für die richtige Dosierung sind sie daher auf Nahrungsergänzungsmittel mit korrekt angegebenen Calciumgehalt angewiesen. In diesem Zusammenhang führen Hersteller von Nahrungsergänzungsmitteln Konzentrationsbestimmungen an ihren Produkten im Rahmen von Qualitätskontrollen durch. Auf der Anfrage eines solchen Herstellers basiert der Praxisanteil dieses Artikels.
Häufig sind calciumhaltige Nahrungsergänzungsmittel in Tablettenform erhältlich, wobei das Calcium als Calciumcarbonat oder Calciumcitrat enthalten ist. Letzteres ist einfacher zu verstoffwechseln, aber auch teurer und hat einen geringeren Calciumanteil. Daher ist Calciumcarbonat die am häufigsten verwendete Verbindung in solchen Produkten.
Was ist eine ionenselektive Elektrode – ein kleiner Exkurs vorab.
Die Messung mit einer ionenselektiven Elektrode ist sehr empfindlich und auch bei geringen Ionenkonzentrationen genau. Eine ISE basiert auf dem Prinzip, dass bei dem Vorhandensein von bestimmten Ionen, nämlich die für die die Elektrode ausgelegt ist, ein konzentrationsabhängiges elektrisches Potential gegenüber einer Referenz aufgebaut wird. Die bekannteste und am weitesten verbreitet ISE ist die pH-Elektrode, die auf Protonen (Wasserstoff- oder Hydroniumionen) anspricht.
Es gibt drei Hauptarten von ISE, die entweder als kombinierte Elektroden mit integrierter Referenz oder als Halbzellen mit externer Referenzelektrode verfügbar sind.
Feststoffelektroden
Eine Feststoffelektrode baut eine Spannung durch Ionenaustausch zwischen Probe und der anorganischen Membran auf. Dadurch, dass das Membranmaterial nur sehr schlecht in der Probe löslich ist, sind solche Elektroden lange haltbar. Feststoffelektroden verwenden kristalline Membranen, die entweder aus Einkristallen oder polykristallinen Pulvern gepresst bzw. aus der Schmelze gegossen werden. Verwendet werden leitfähige Kristalle, die sich dadurch auszeichnen, dass sie ein Ion besitzen, das im Festkörper beweglich ist. Ein Beispiel ist die von Hanna Instruments hergestellte Elektrode aus Silbersulfid (Ag2S) mit beweglichem Silberion Ag+. Sie ist sowohl für Silber wie auch für Sulfid-Ionen sensitiv ist.
Flüssigkeitsmembranelektroden
Eine Flüssigkeitsmembranelektrode verfügt über eine dünne PVC-Folie als Membran, die mit einem Ionophor – einem Molekül, das in der Lage ist spezifische Ionen zu binden und durch Membranen zu transportieren – beschichtet ist. Eine der ersten Elektroden dieser Bauart ist die Kalium-ionenselektive Elektrode, bei der die Membran mit dem Antibiotikum Valinomycin als Ionophor beschichtet ist. Die Valinomycin-Moleküle sind in der Lage K+-Ionen mit ihrer ringförmigen Struktur einzufangen und sie nach Transport durch die Membran wieder freizusetzen. Da diese Elektrodensorte mechanisch wesentlich empfindlicher als eine Feststoffelektrode ist, sind die Sensormodule einfach austauschbar.
Gasmembranelektroden
Gasmembranelektroden sind stets kombinierte Elektroden. Sie dienen der Messung gelöster Gase in Flüssigkeiten. Bei diesem Typus trennt eine gasdurchlässige Membran das Sensorelement von der Messlösung. Bedingt durch den Partialdruck des gelösten Gases diffundiert es durch die Membran und ändert dort den pH-Wert eines dünnen Films eines ungepufferten Elektrolyten auf der Oberfläche des internen pH-Sensors. Die Diffusion läuft solange ab, bis ein Gleichgewicht der Partialdrücke in Elektrolyt und Messlösung erreicht ist. Der pH-Wert ist proportional zur Menge gelösten Gases in der Probe. Hanna Instruments stellt Gasmembran-ISE für Kohlendioxid und Ammoniak her.
Wie kann mit einer ionenselektiven Elektrode gemessen werden?
Eine ISE kann sowohl für absolute wie auch relative Messmethoden verwendet werden. Zu den relativen Messmethoden zählen alle Messmethoden, die Standards verwenden. Das gemessene Elektrodenpotential wird dabei in Relation zu den bekannten Konzentrationen der Standards gesetzt. Die externe Kalibrierung z.B. wird vor den direkten potentiometrischen Messungen durchgeführt. Bei absoluten Methoden wird das Signal der Elektrode ohne vorhergehenden Kalibrerung benutzt. Beispiel hierfür ist die potentiometrische Titration mit einem bestimmten ISE-Signal bzw. einer Signaländerung als Indikator für den Endpunkt.
Beide Vorgehensweisen haben Ihre Vor- und Nachteile, die in Bezug auf die Messung mit ISE im Folgenden kurz diskutiert werden. Eine allgemeine Diskussion wird auf einen weiteren Blog-Beitrag vertagt, da dieses Thema von grundlegendem Interesse ist und dementsprechend gewürdigt werden sollte.
Direkte Potentiometrie
Die Kalibrierung mit Standardlösungen separat von den Proben (extern) ist die am häufigsten verwendete Kalibriermethode. Die direkte Potentiometrie bietet sich vor allem für den Routinebetrieb mit vielen ähnlichen Proben an. Messgeräte wie das Labormessgerät HI5522 zeigen die Ionenkonzentration einer unbekannten Probe direkt an, nachdem das Instrument mit zwei oder mehr Standards kalibriert wurde. Anpassungen der Ionenstärke werden für Standard und Messprobe durchgeführt. Diese Variante gestattet schnelle, routinemäßige Messungen für eine Reihe unterschiedlicher Applikationen.
Als alternative, relative Messmethode bietet sich die Kalibrierung mit internen Standards an. Bei der internen Standardisierung wird der Standard zur Messprobe gegeben, das heißt, die Probe wird ein oder mehrfach mit bekannten Mengen an Standard aufgestockt. Die Konzentration der ursprünglichen Probe wird durch eine Regression (Kalibriergerade) ermittelt. Diese Methode bietet den Vorteil, dass sie weniger fehleranfällig ist, weil sich Einflüsse bei der Messung durch Variablen wie pH, Viskosität, Ionenstärke und Matrix aufheben.
Potentiometrische Titration
Bei der potentiometrischen Titration werden ISE üblicherweise zur selektiven Detektion, entweder von einem Titrantenbestandteil oder von einer Probenspezies eingesetzt. Somit kann der Verlauf einer z.B. Fällungs- oder komplexometrischen Titration verfolgt und der Endpunkt detektiert werden. Der Endpunkt der Titration wird durch das Erreichen eines bestimmten Spannungswerts bzw. -änderung bestimmt. Bei der Verwendung von ISE als Indikator für den Titranten erfolgt z.B. ein sprunghafter Spannungsanstieg dann, wenn der Analyt in der Probe vollständig ausgefällt (aufgebraucht) wurde und dadurch die Konzentration des Titranten in der Messlösung schlagartig ansteigt.
Was macht hier Sinn – Direktmessung oder Titration?
Prinzipiell sind beide Vorgehensweisen für die Messung des Calciumgehalts in den Nahrungsergänzungsmitteln durchführbar. Die potentiometrische Titration bietet den Vorteil, dass hier lediglich die Änderung des Elektrodensignals zu Endpunktdetektion verwendet werden kann. Es entfällt also die Notwendigkeit der Kalibrierung mit Standards, was mit Aufwand verbunden ist, da Standards frisch hergestellt und die Elektrode täglich kalibriert werden muss. Insbesondere der Aufwand für die interne Standardisierung ist in diesem Fall unnötig, da die zu untersuchenden Proben in der Regel keine komplexe Matrix aufweisen. Die Wahl fiel also auf die potentiometrische Titration, auch da nur eine überschaubare Anzahl an Proben pro Tag gemessen werden sollte.
Vorgehensweise bei der titrimetrischen Bestimmung von Calcium
Calcium wird mittels komplexometrischer Titration bestimmt, dabei wird EDTA (Ethylendiamintetraessigsäure) als Komplexbildner eingesetzt. Das bedeutet, EDTA entzieht der Probe Ca2+-Ionen, die in einem Komplex gebunden werden. Es wird also so lange EDTA-Lösung zugegeben, bis das gesamte in der Probenlösung vorhandene Calcium verbraucht ist. An diesem Punkt wird sich das Signal der Calcium-ISE nicht mehr ändern und die Titration beendet. Aus dem Verbrauch an EDTA bis zum Erreichen dieses Punkts lässt sich dann einfach auf die Calciumkonzentration schließen.
Bei den zu untersuchenden Proben handelte es sich um Tabletten. Um das Calcium für die Messung aufzuschließen werden die gemörserten Tabletten in Salzsäure aufgelöst. Danach wird der pH-Wert der Lösung mittels eines Ammoniumchlorid / Ammoniumhydroxid-Puffers auf 10 eingestellt. Die Komplexbildung mit EDTA erfolgt am besten bei pH-Werten zwischen 9 und 11. Für die Durchführung der Titration wurde das Gespann aus Hannas potentiometrischem Titrator HI932 und der Calcium-Kombinations-ISE HI4104 verwendet. Durch die hohe Genauigkeit der 40.000-Schritt-Kolbendosierpumpe des Titrators und die Geschwindigkeit des dynamischen Dosierverfahrens, kann der Titrationsendpunkt sowohl schnell als auch präzise bestimmt werden. Bei der dynamischen Dosierung wird das EDTA anfangs in größeren Voluminaschritten zudosiert und es wird automatisch umso feiner dosiert je näher man dem Endpunkt kommt, so dass dieser exakt erkannt werden kann und die Analysezeit trotzdem kurz bleibt.
Somit ist die titrimetrische Bestimmung von Calcium mit einer ISE als Indikator eine einfach anzuwendende und genaue Messmethode, die den Ansprüchen an die routinemäßige Überprüfung einer kleineren Anzahl von Proben – wie hier Nahrungsergänzungmitteln – mehr als genügt. Haben Sie Fragen dazu, ob ein ähnliches Verfahren für Ihre Problemstellung verwendet werden kann?
Literaturhinweise
[1] chemgapedia.de, Artikel zu Kalibrierung, Zugriff am 18.08.2017
[2] Douglas A. Skoog und James J. Leary, Instrumentelle Analytik: Grundlagen – Geräte – Anwendungen, Springer, 1996
Autoren: Stefan Langner und Dr. Eugen Federherr.
Aus Gründen der sprachlichen Vereinfachung wird auf die Nennung der Geschlechter verzichtet, wo eine geschlechtsneutrale Formulierung nicht möglich ist. In diesen Fällen beziehen die verwendeten männlichen Begriffe die weiblichen Formen ebenso mit ein.
Haben Sie Fragen oder Anregungen?
Haben Sie noch Fragen oder Anregungen zum Artikel, zu den Produkten oder ganz allgemein? Kontaktieren Sie uns über unser Kontaktformular, schreiben Sie uns eine E-Mail oder besuchen Sie uns auf unseren Seiten in den sozialen Medien. Unsere Mitarbeiter sind gern für Sie da.
Zugehörige Produkte

Ionenselektrive Elektrode, Polymermembran, Kombination aus PEI/PVC, ausgelegt für die Bestimmung von freiem Kalzium in Getränken, Süßwasser und Meerwasser. Messbereiche 1 M bis 3 x 10-6 M40080 bis 0,12 mg/L Optimaler pH-Bereich 4 - 10 Temperaturbereich 0 - 40 °C Ungefähre Steilheit +28 Korpusmaterial PEI/PVC Kabel Koaxial 1m mit BNC-Anschluss Abmessungen Ø 12 mm x 120 mm (Eintauchtiefe)




